注重皮肤健康的你,是否正通过敷胶原蛋白面膜、吃鸡爪猪脚、喝燕窝或胶原蛋白饮来“补胶原”? 但这些方法真的有效吗?
胶原蛋白约占人体总蛋白的25%,是含量最丰富的结构蛋白,广泛存在于皮肤、骨骼、肌腱、血管等组织中,对维持身体结构与功能至关重要。目前已发现28种类型(I–XXVIII型),其中I型和III型占比高达95%。
天然胶原蛋白由三条约1014个氨基酸组成的α链构成,形成独特的三螺旋结构,分子量约300 kDa。这一结构赋予其多重生理功能:提升皮肤弹性与保水力、促进伤口愈合、强健关节骨骼、改善发质指甲,甚至保护视力。
——但补充方式是否科学,决定了效果能否真正落地。
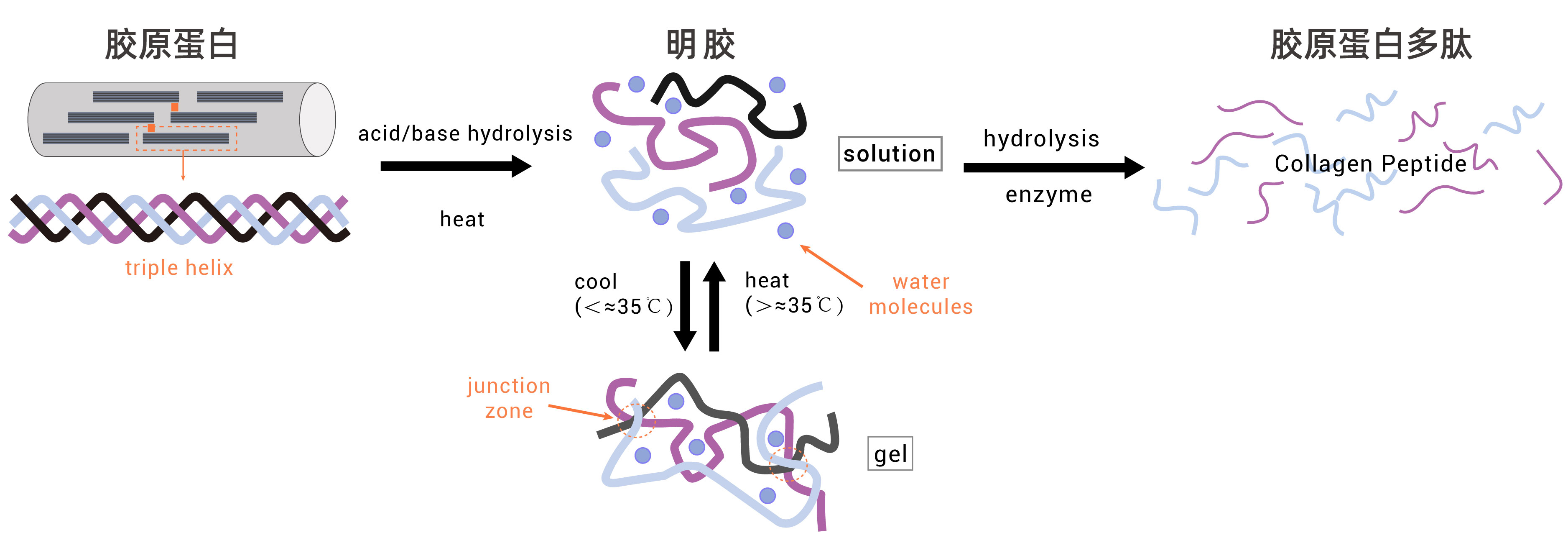
如上图所示,胶原蛋白类产品广义上可分为三类:胶原蛋白、明胶和胶原多肽。
天然胶原蛋白在酸/碱及热作用下部分水解生成明胶——鸡爪、猪蹄、皮冻、阿胶等所含的主要成分即为此;明胶再经酶解可进一步降解为胶原多肽,这也是多数面膜和口服液的核心成分。
全球胶原蛋白市场持续增长。据Grand View Research数据,2022年市场规模达172.58亿美元,预计2027年将增至226.22亿美元(CAGR 5.42%)。其中,医疗健康(预计2027年达111.17亿美元,占比约50%)是主要增长引擎,其次为美容护肤与食品饮料。不同应用领域对应不同的法规与质量标准,而随着技术进步,胶原蛋白的应用边界仍在不断拓展。
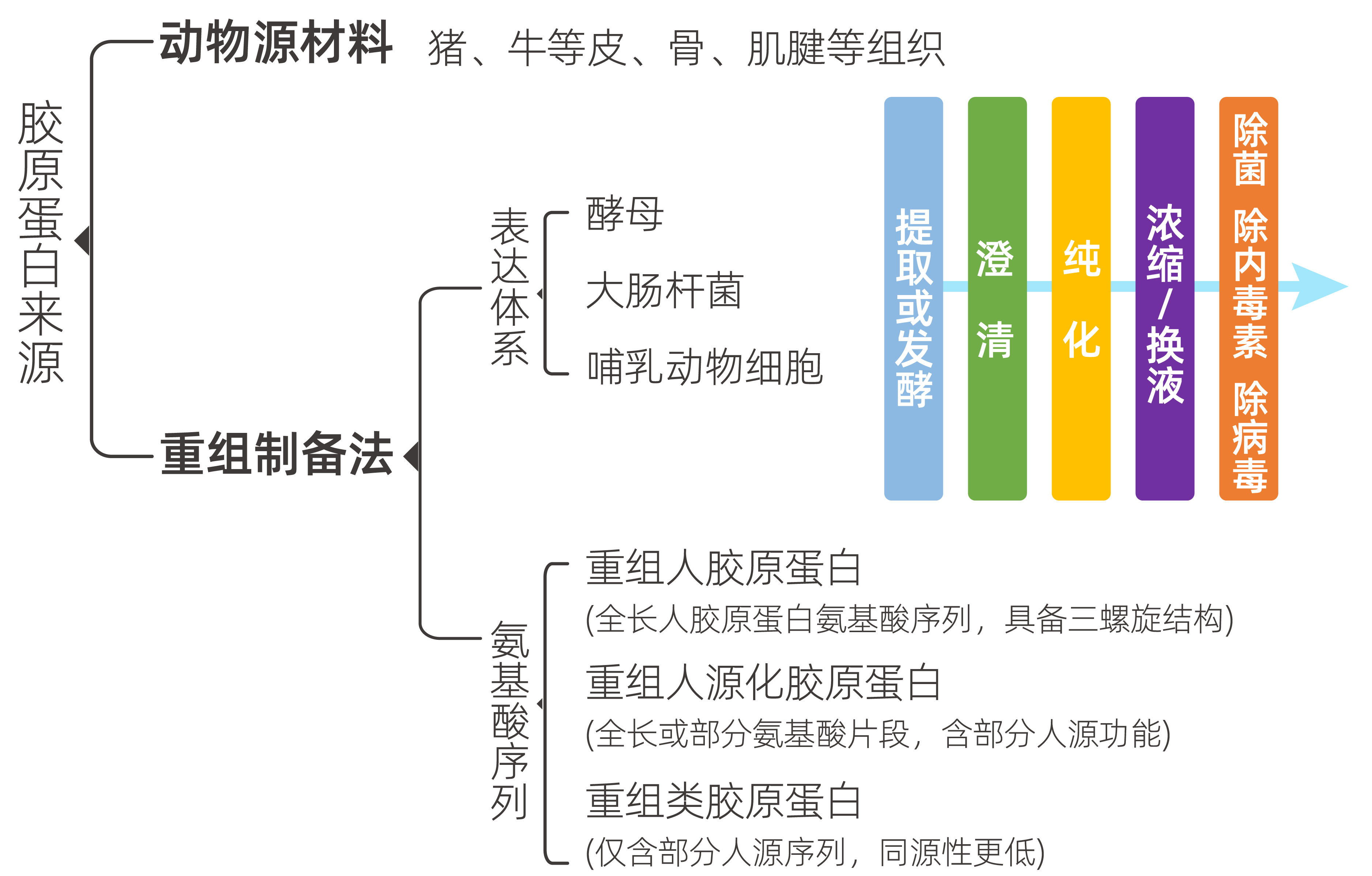
目前,胶原蛋白制备主要分为动物源提取和重组表达两大路径。根据国家药监局2021年《重组胶原蛋白生物材料命名指导原则》,重组胶原蛋白分为三类:
·重组人胶原蛋白(具完整三螺旋结构)
·重组人源化胶原蛋白(含部分人源序列)
·重组类胶原蛋白(同源性较低)
常用表达体系包括大肠杆菌、酵母及哺乳动物细胞(如CHO)。尽管工艺细节因来源和体系而异,但整体流程通常包括:发酵/提取 → 澄清 → 纯化(去除杂质、内毒素、病毒等)→ 换液/浓缩 → 除菌过滤等关键步骤。
澄清
在提取或发酵后的澄清阶段,以及纯化过程中沉淀或酶解后的料液,通常浊度较高,含有细胞、碎片、沉淀物等杂质,需通过澄清工艺保障后续步骤顺利进行。
鉴于操作便捷性与澄清效果,深层过滤是优先选择。针对料液的复杂性和不同工艺需求,科百特提供多种精度与特性的深层过滤方案,灵活适配各工艺环节。
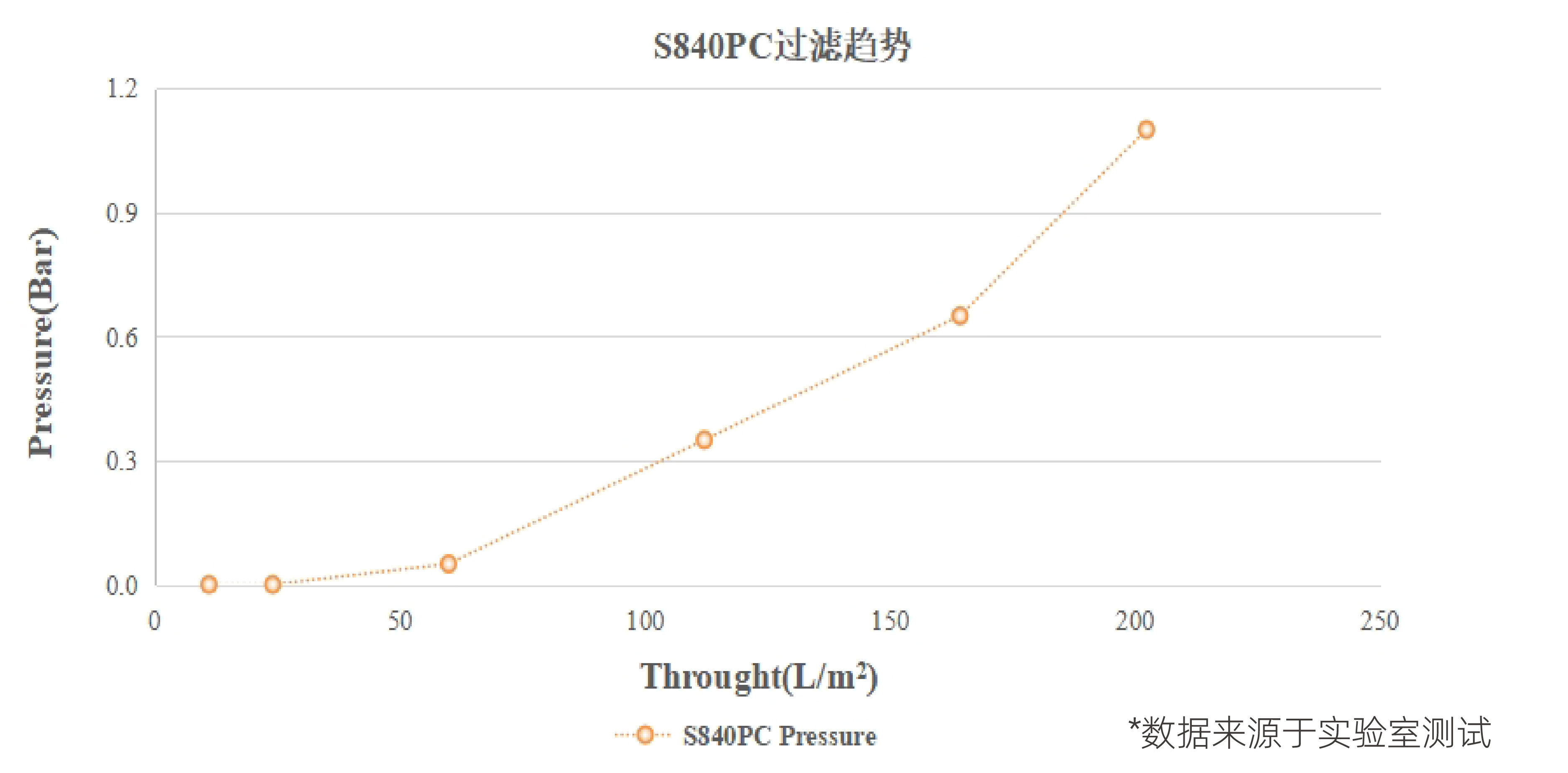
以某CHO表达的胶原蛋白项目为例:
CHO细胞发酵液,经酶解+调pH,静置过夜后上清液,初始浊度>300 NTU
型号 | 过滤总量 (g) | 平均通量 (LMH) | 终点压差 (bar) | 载量 (L/m²) | 混合浊度 (NTU) | 收率% |
1*S840PC | 467.15 | 256 | 1.1 | 203 | 1.07 | 94.75 |
对于部分工艺考虑耗材重复使用和固含量过高的步骤,如酵母体系发酵后,也可以选择微滤中空纤维或膜包进行澄清,具体案例如下:
酵母发酵表达重组人源化胶原蛋白,离心后料液浊度147 NTU,选择中空HFEMIN0201030P测试,即0.2μm孔径,1mm内径的微滤中空进行测试,结果如下:
| 测试 | 进液流量 (ml/min) | 剪切速率 (S-1) | TMP (psi) | 时间 (min) | 浓缩/洗滤 倍数 | 平均滤速 (LMH) | 透过液浊度 (NTU) |
| 浓缩 | 282 | 6000 | 0.75 | 170 | 5.77 | 30.77 | 3.41 |
| 洗滤 | 282 | 6000 | 0.75 | 167 | 6 | 28.67 | 3.41 |
料液经约6倍浓缩,换液6倍,通量维持在较高水平~30LMH,滤后浊度3.41NTU,澄清效果良好,同时在回流端未检测到目的蛋白,证明对目的物无显著吸附或截留;
纯化
传统层析填料成本较高,且在处理高粘度物料时易缩短使用寿命;同时,其操作通常依赖大型层析系统,对设备投入、厂房空间及布局提出更高要求。
因此,行业正逐步转向膜层析技术:凭借更高载量、更快流速和更强纳污能力,膜层析可显著减少耗材用量、缩短工艺时间,并省去装柱、拆柱及保存等繁琐步骤,操作更灵活,占地更小。
在某重组I和III型胶原蛋白纯化工艺中,阴离子纯化步骤分别对比传统填料和科百特膜层析Pultrix™ XQ的工艺表现,膜层析载量(60g/L)可以达到传统层析填料(15g/L)的4倍,HCP去除可以达到95%以上。在收率方面I型胶原蛋白的膜层析可以达到90%,而传统填料仅约60%;III型胶原蛋白收率也比传统填料提高5%,如下图所示。
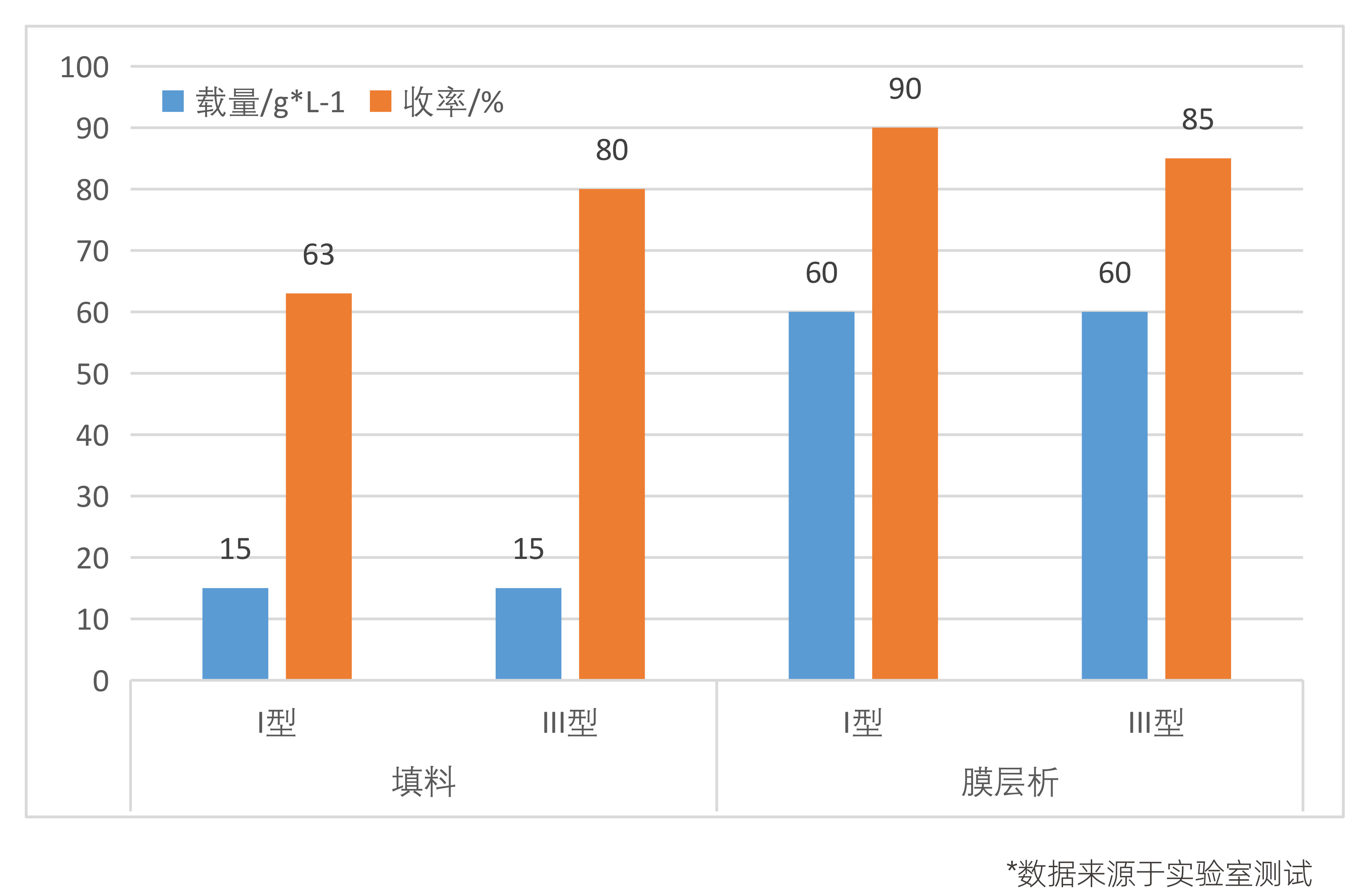
基于客户工艺需求,科百特提供多种机理的膜层析产品,包括阴离子交换(AEX)、阳离子交换(CEX)和疏水相互作用(HIC)等。其中,AEX膜层析除上述纯化工艺外,也广泛用于内毒素去除等关键步骤。
浓缩/换液
常规换液与浓缩可选用超滤膜包或中空纤维。但对于动物源胶原蛋白等高粘度物料,浓缩后粘度显著升高,对除菌过滤构成严峻挑战。建议采用灭菌级中空纤维:先在低浓度下完成除菌过滤,再通过无菌连接转入无菌中空纤维系统进行浓缩至目标浓度,从而有效提升工艺效率与产品收率。
某动物来源胶原蛋白产品,分子量300kD以上,初始浓度1.0mg/mL,期望通过超滤浓缩至5-10.0mg/mL。实验测试了科百特超滤膜包UFCLA0100001P(RC材质,常规流道,100kD),工艺为先透析除杂4倍,再浓缩5倍,透析过程平均通量为137.44LMH,浓缩过程平均通量为114.26LMH。
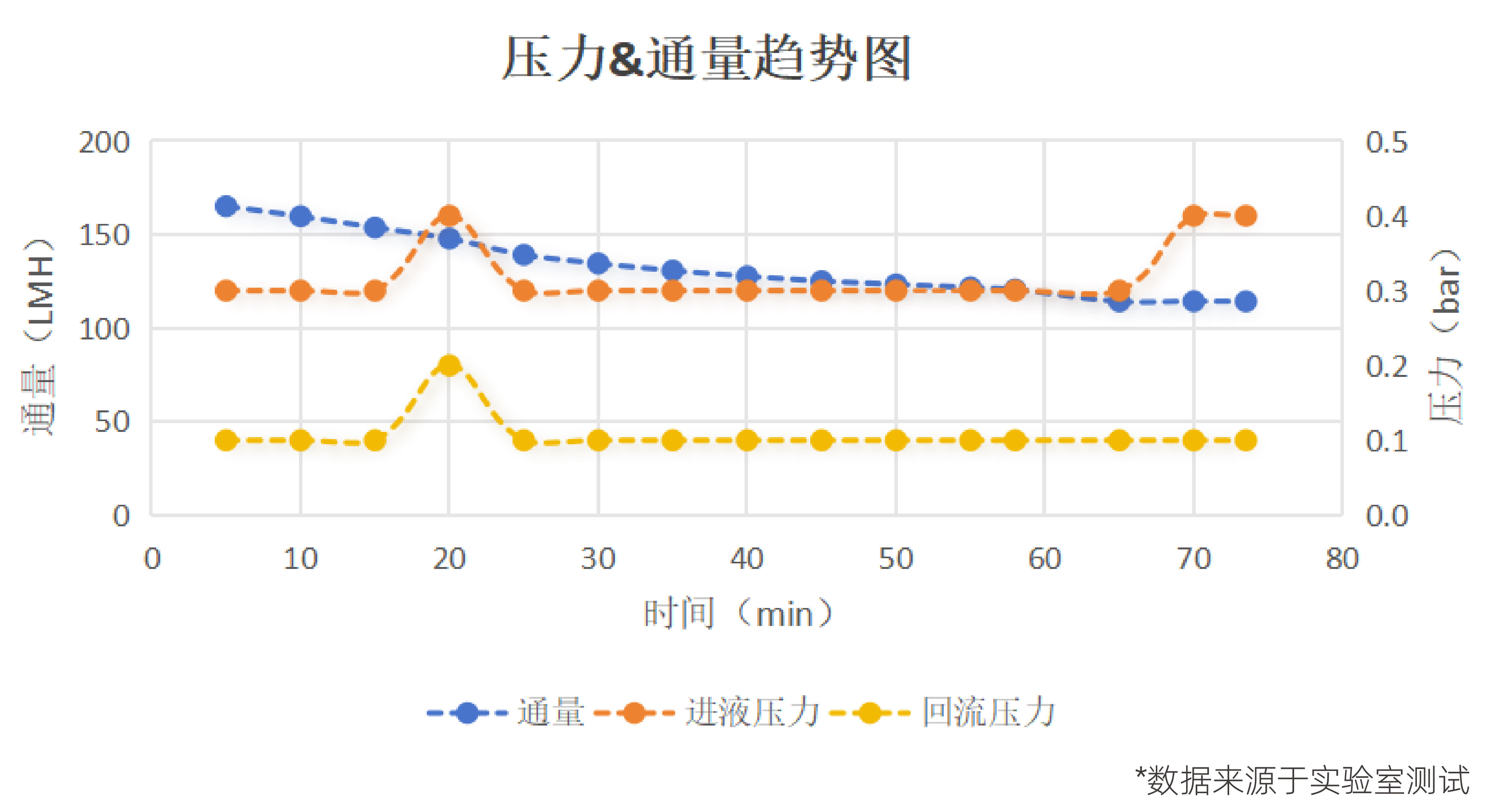
某天然胶原蛋白产品,目标蛋白分子量300kd,希望通过切向流过滤去除小分子杂质,同步对比了100K膜包(常规流道)和中空纤维(0.5mm内径)的表现,透析换液过程中压力和流速表现如下图:
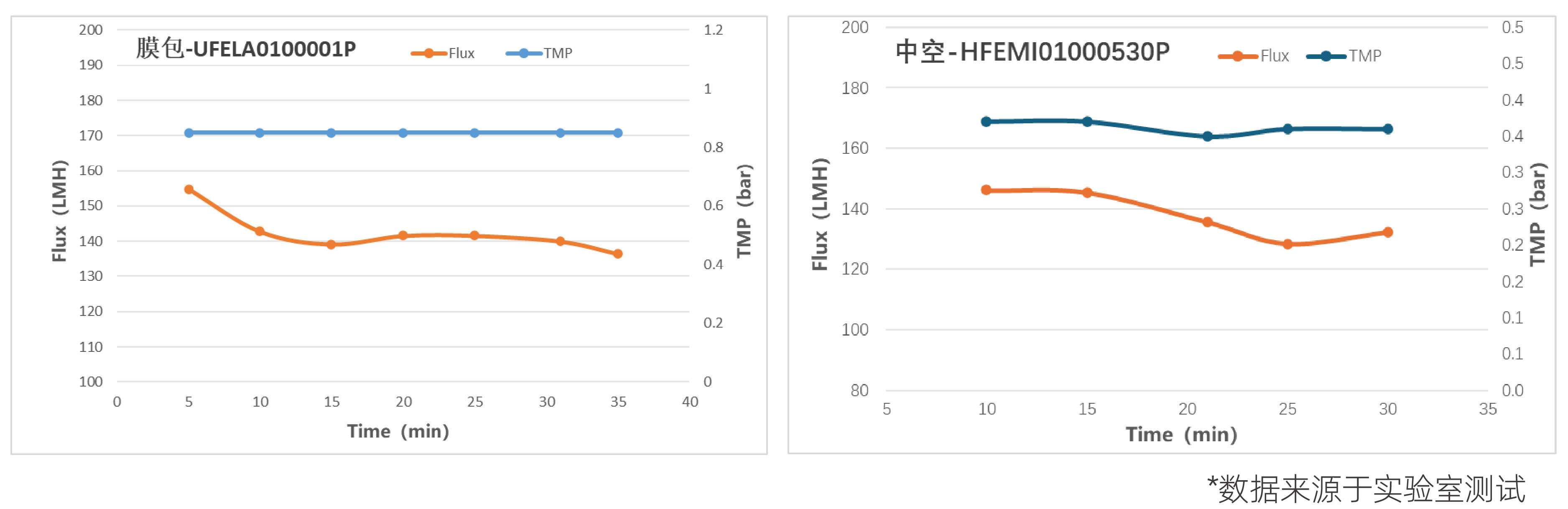
耗材 | 进口流速 | TMP (bar) | 时长 (min) | 透析 倍数 | 平均滤速 (LMH) |
膜包 | 5LMM | 0.85 | 35 | 8.31 | 142.46 |
| 中空纤维 | 4000S-1 | 0.35 | 30 | 8.51 | 144.24 |
由上表可知,无论是膜包还是中空纤维均在换液除杂过程表现出较高的工艺通量,且清洗后水通量恢复95%以上,可以满足客户在较短时间内完成预定工艺,并可以重复使用,有效降低生产成本。
除病毒
除病毒滤器的载量和选型与目标蛋白分子量密切相关:
· 对于 200 kDa 以下的重组胶原蛋白,可首选 PES 材质滤器(如 ViruClear™ VF 或ViruClear™ VF Plus)
· 而 200 kDa 以上或全长序列的胶原蛋白,因分子量大、粘度高,易导致 PES 滤器堵塞、载量偏低,建议采用纤维素材质 滤器(如 ViruClear™ RCH),其具备更高载量和更小流量衰减。
目前,已有客户在 6000 L 生产规模的除病毒工艺中成功应用 RCH。
在另一客户案例中,原工艺采用国外除病毒,收率仅为30%,通过优化滤器(预过滤和除病毒过滤),收率可以达到约90%。
除菌
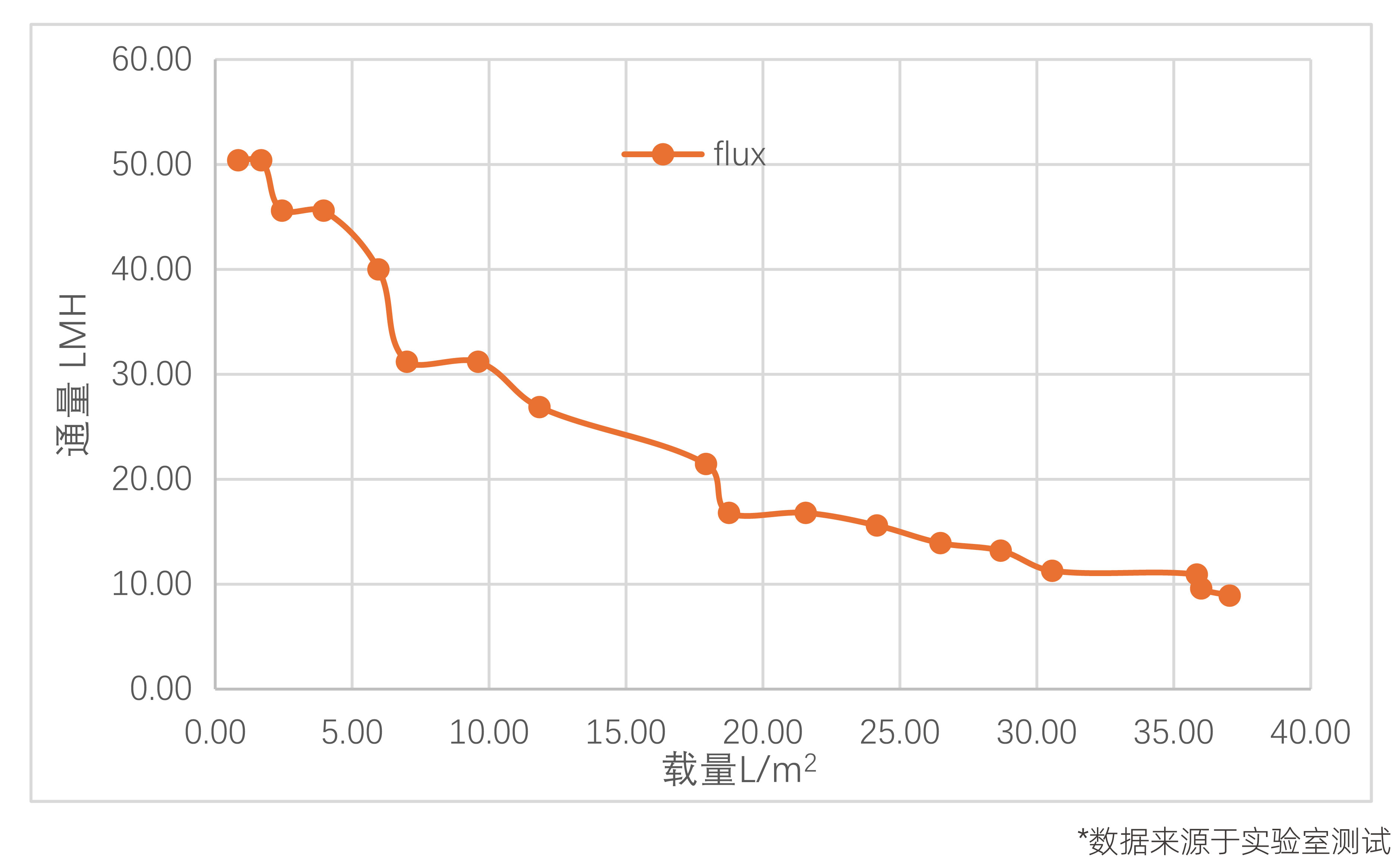
某酵母发酵体系表达的人源化胶原蛋白项目中,对于除菌过滤工艺,考察不同蛋白浓度的影响,选用科百特PVDF材质滤器LHPVND0022分别过滤15g/L(左下图)和40g/L(右下图)的料液,实验结果如下:
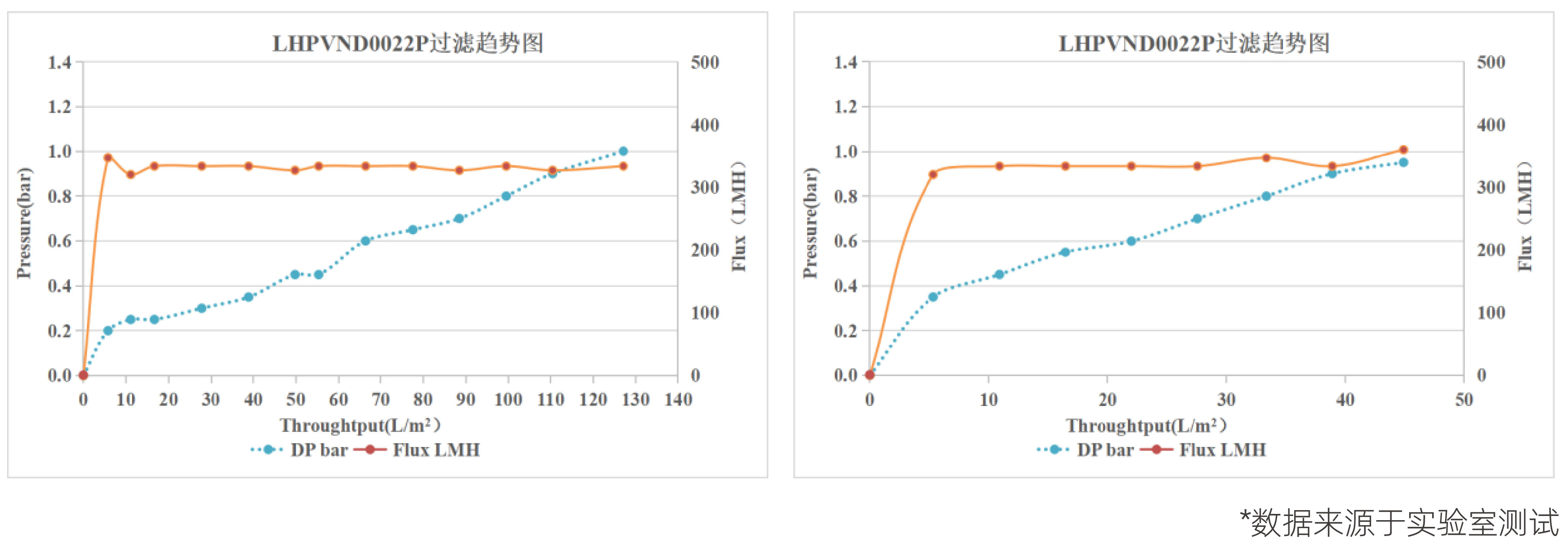
本案例中浓缩后料液的除菌载量往往较低(约45L/m2),而未浓缩或浓度较低的料液,载量可以提升至3倍(约130L/m2)。所以,如前文所述,可以考虑在工艺设计时先进行除菌过滤,再通过无菌款中空实现浓缩至目标浓度,具体设计时可以基于成本、风险、灵活度等维度进行综合考量。其次,在设计上也可以考虑组合过滤,通过适宜的预过滤提高除菌滤器的载量。
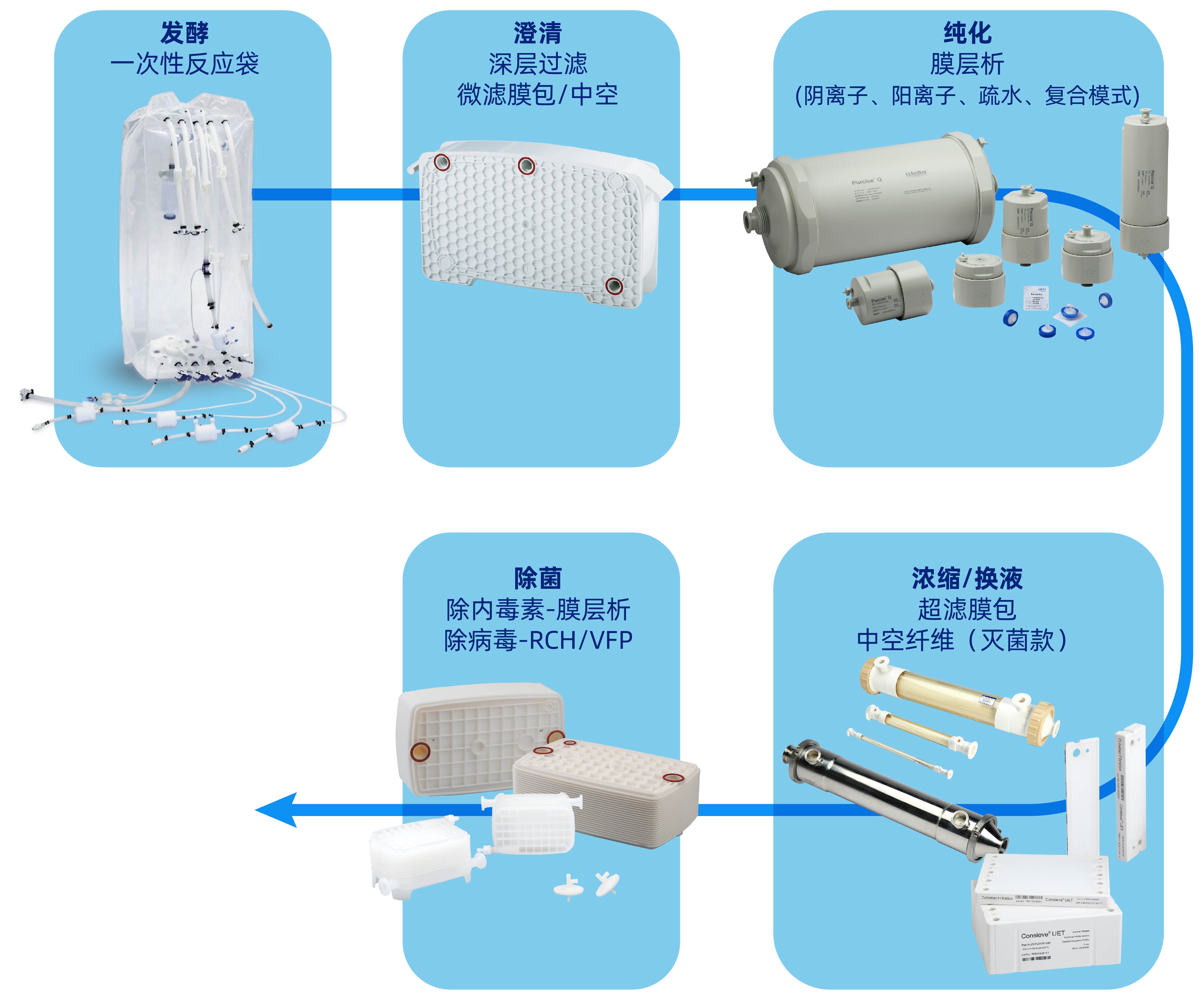
本文旨在介绍科百特从上游到下游的胶原蛋白全链条解决方案,结合典型案例与关键难点分析,为您的工艺路线优化提供更具价值的思路,助力胶原蛋白生产工艺升级。
需特别说明的是,由于胶原蛋白来源多样、分子量差异显著,且工艺路线各不相同,实际应用中常面临不同的技术瓶颈。